불화 알루미늄
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
불화 알루미늄(AlF3)은 알루미늄과 불소로 이루어진 화합물이다. 주로 알루미나를 플루오린화 수소와 반응시켜 생산하며, 육불화규산 또는 육불화알루민산 암모늄의 열분해를 통해서도 얻을 수 있다. 무수 형태 외에도 다양한 수화물이 존재하며, X선 결정학에 따르면 무수 불화 알루미늄은 뒤틀린 팔면체를 특징으로 하는 구조를 갖는다. 불화 알루미늄은 알루미늄 생산 시 크라이올라이트와 함께 용융점을 낮추고 전도성을 증가시키는 첨가제로 사용되며, 생물학적 인산기 전달 반응 연구, 플루오로알루미네이트 유리 생산, 광학 박막 등 다양한 분야에 응용된다. 유해 물질로 반복적 또는 장기간 흡입 시 천식, 뼈 변형, 신경계 손상을 유발할 수 있으며, 대한민국 환경부는 불화 알루미늄을 유해화학물질로 지정하여 관리하고 있다.
더 읽어볼만한 페이지
- 알루미늄 화합물 - Alq3
트리스(8-히드록시퀴놀리네이트)알루미늄(Alq₃)은 자오면 및 안면 이성질체와 여러 다형체를 가지며, 유기 발광 다이오드(OLED)의 전자 수송층 물질로 널리 쓰이고 퀴놀린 고리의 치환기 변화를 통해 발광 특성 조절이 가능하다. - 알루미늄 화합물 - 녹주석
녹주석은 육방정계에 속하는 규산염 광물로, 다양한 색상을 띠며 베릴륨 화합물로 알려져 채굴, 취급, 정제 시 폐렴을 유발할 수 있다. - 플루오린화물 - 헥사플루오로인산
- 플루오린화물 - 아불화 은
아불화 은은 아이오딘화 카드뮴과 결정 구조는 같지만 이온 위치가 반대이며, 은 원자 간 최단 거리는 299.6 pm이다. - 금속 할로젠화물 - 염화 칼륨
염화칼륨(KCl)은 칼륨 이온과 염화물 이온으로 이루어진 이온성 화합물로, 칼륨 비료, 화학 공업, 의학, 사형 집행 등 다양한 용도로 사용되며, 면심입방구조와 광학적 특성을 지니고, 캐나다, 러시아, 벨라루스 등에서 주로 생산된다. - 금속 할로젠화물 - 염화 나트륨
염화 나트륨은 염화물 이온과 나트륨 이온으로 구성된 백색 고체 이온 결정으로, 짠맛을 내며 융점은 800.4℃이고, 다양한 용도로 사용되며 겨울철 제설에도 활용되는 정염의 일종이다.
2. 생성
대부분의 불화 알루미늄은 700°C에서 알루미나를 플루오린화 수소로 처리하여 생산된다.[10] 또한 육불화규산을 이용하여 제조할 수도 있다.[11]
:H2[SiF6] + Al2O3 + 3 H2O → 2 AlF3 + SiO2 + 4 H2O
다른 방법으로는 육불화알루민산 암모늄을 열분해하여 얻는 방식이 있다.[12] 실험실 규모의 소량 제조 시에는 수산화 알루미늄 또는 금속 알루미늄을 플루오린화 수소와 반응시켜 만들기도 한다.
2. 1. 자연 발생
불화 알루미늄 삼수화물은 희귀 광물인 로젠베르기트로 자연에서 발견된다. 무수 형태는 비교적 최근(2020년 기준)에 알려진 광물인 오스카르손나이트로 나타난다.[13][14] 관련 희귀 광물로는 화학식 Al(OH)2F를 가지는 자르치키트가 있다.[15][14]3. 구조
X선 결정학에 따르면, 무수 AlF3는 뒤틀린 AlF6 팔면체 구조 단위들이 산화 레늄과 유사한 배열(모티프)을 이루고 있다. 각 플루오라이드 이온은 두 개의 알루미늄(Al) 중심과 연결되어 있다. 이러한 3차원 고분자 구조는 AlF3가 높은 융점을 갖게 하는 원인이 된다. 이는 고체 상태에서 다른 알루미늄 삼할로겐화물들과는 다른 구조적 특징이다. 예를 들어, AlCl3는 층상 구조를 가지며, AlBr3과 AlI3는 분자 이합체 형태로 존재한다.[16] 이들 염화물, 브롬화물, 요오드화물은 상대적으로 낮은 융점을 가지며 쉽게 증발하여 이합체를 형성하는 경향이 있다.[17]
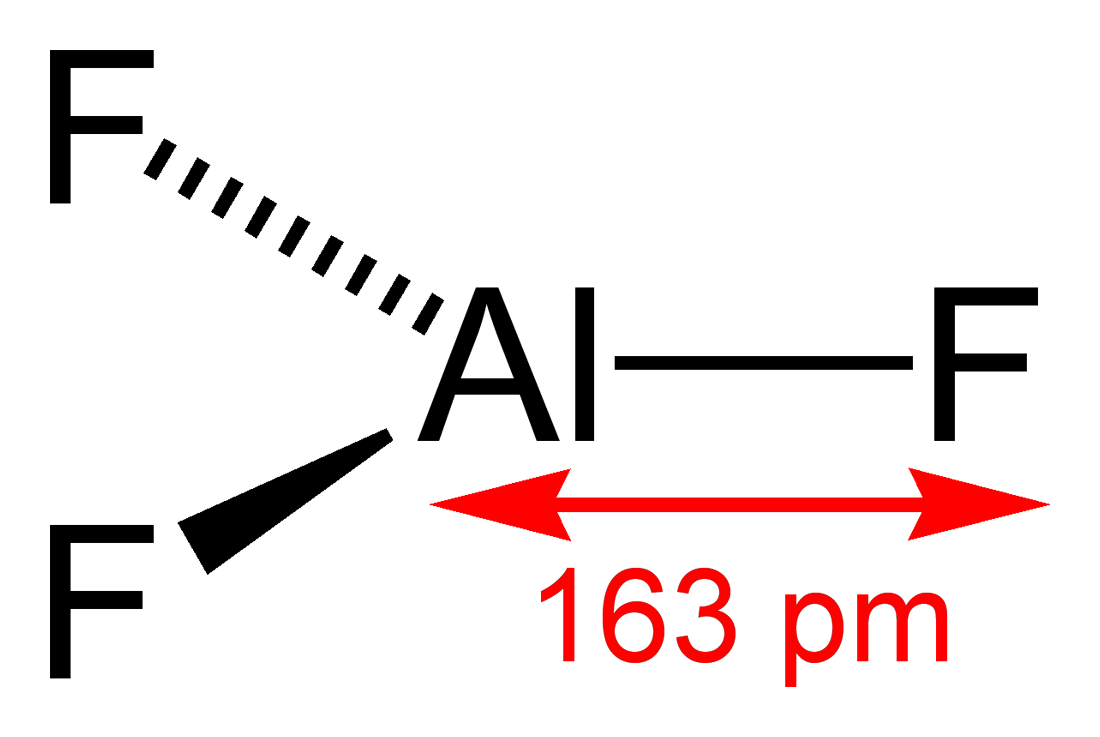
기체 상태에서 불화 알루미늄 분자(AlF3)는 ''D''3h 점군 대칭성을 가지는 삼각 평면 구조로 존재한다. 이 기체 분자에서 알루미늄과 플루오린 사이의 결합 길이(Al–F)는 163pm이다.
4. 응용
불화 알루미늄은 전기 분해를 통한 알루미늄 생산에 중요한 첨가제이다.[10] 크라이올라이트와 함께 용융점을 1000°C 이하로 낮추고 전해질의 전도성을 증가시킨다. 산화 알루미늄(알루미나)는 이 용융된 염에 용해된 후 전기 분해되어 대량의 알루미늄 금속을 생성한다.[12]
4. 1. 기타 응용
불화 알루미늄 복합체는 생물학적 인산기 전달 반응의 메커니즘을 연구하는 데 사용된다. 이는 세포 활동에 매우 중요한데, 아데노신 삼인산(ATP) 및 구아노신 삼인산(GTP)과 같은 물질이 생물의 신진대사, 성장, 분화 등 대부분의 반응을 조절하기 때문이다.[18] 특히 불화 알루미늄이 헤테로트리머 G 단백질에 결합하여 이를 활성화시킬 수 있다는 사실이 밝혀지면서, 생체 내 G 단백질 활성화 연구, 여러 GTPase의 3차원 구조 규명, 그리고 GTPase 활성 단백질(GAP)의 역할을 포함한 GTP 가수분해 메커니즘을 이해하는 데 유용함이 입증되었다.[19]지르코늄 플루오라이드와 함께 플루오로알루미네이트 유리 생산에 사용된다.
또한 발효를 억제하는 용도로도 쓰인다.
플루오린화 마그네슘과 마찬가지로 낮은 굴절률을 가지므로 광학 박막 재료로 사용된다. 특히 자외선 중에서도 파장이 짧은 원자외선 영역의 빛을 잘 통과시켜야 하는 경우에 유용하다. 이러한 박막은 주로 물리적 기상 증착(PVD) 방식으로 증착하여 제작한다.
5. 안전성
불화 알루미늄은 유해 물질로 분류되며, 반복적이거나 장기간 흡입 노출 시 천식을 유발할 수 있고, 뼈와 신경계에 영향을 미쳐 뼈 변형(불소증) 및 신경계 손상을 일으킬 수 있다.[21][36] 보고된 경구 동물 치사량(LD50)은 100mg/kg이다.[20]
불소의 여러 신경독성 효과는 불화 알루미늄 복합체 형성 때문에 나타난다. 이 복합체는 인산염의 화학 구조와 유사하여 ATP 포스포하이드롤라아제 및 포스포리파아제 D의 활성에 영향을 미친다. 불화 알루미늄 복합체는 매우 적은 마이크로몰 농도의 알루미늄만으로도 형성될 수 있다.[22]
인체가 불화 알루미늄에 노출되는 경우는 주로 알루미늄 환원 공정과 같은 산업 현장에서의 배출[23] 또는 불소와 알루미늄을 함께 섭취할 때 발생할 수 있다. 불소는 식수나 불소 기반 농약 잔류물 등을 통해 섭취될 수 있으며, 알루미늄은 식수, 차, 식품 잔류물, 유아용 조제 분유, 알루미늄 함유 제산제나 약물, 데오도란트, 화장품, 유리 제품 등을 통해 노출될 수 있다.[22] 또한, 불소화된 다른 화학 물질에도 불화 알루미늄이 포함될 수 있다.[24] 물 속에 존재하는 알루미늄 화합물에 만성적으로 노출되었을 때 나타날 수 있는 신경 독성 효과에 대한 연구는 아직 제한적이다.[25]
참조
[1]
서적
RubberBible92nd
[2]
서적
CRC Handbook of Chemistry and Physics
https://books.google[...]
CRC Press
2003-06-19
[3]
서적
RubberBible92nd
[4]
논문
Zur kenntnis von AlF3 und InF3 [1]
[5]
서적
RubberBible92nd
[6]
서적
HazMat Data: For First Response, Transportation, Storage, and Security
https://books.google[...]
John Wiley & Sons
2005-03-04
[7]
웹사이트
Aluminum Fluoride
https://pubchem.ncbi[...]
National Institute of Health
2017-10-12
[8]
간행물
PGCH
[9]
논문
The missing Hydrate AlF3·6H2O [Al(H2O)6]F3: Ionothermal Synthesis, Crystal Structure and Characterization of Aluminum Fluoride Hexahydrate
[10]
서적
Greenwood&Earnshaw2nd
[11]
논문
Manufacture of Aluminium Fluoride of High Density and Anhydrous Hydrofluoric Acid from Fluosilicic Acid
2012-01-01
[12]
간행물
Fluorine Compounds, Inorganic
2005
[13]
웹사이트
Óskarssonite
https://www.mindat.o[...]
[14]
웹사이트
List of Minerals
https://www.ima-mine[...]
2011-03-21
[15]
웹사이트
Zharchikhite
https://www.mindat.o[...]
[16]
문서
REDIRECT
[17]
서적
Inorganic Chemistry
Academic Press
2001
[18]
논문
Signaling mechanistics: Aluminum fluoride for molecule of the year
1997-11-01
[19]
논문
Evidence for distinct mechanisms of transition state stabilization of GTPases by fluoride
1998-03-03
[20]
웹사이트
ALUMINUM FLUORIDE, CASRN: 7784-18-1
https://toxnet.nlm.n[...]
CDC.gov
2005-06-24
[21]
웹사이트
ALUMINIUM FLUORIDE (ANHYDROUS) International Chemical Safety Cards (ICSC)
https://www.cdc.gov/[...]
2015-07-22
[22]
서적
Fluoride in Drinking Water: A Scientific Review of EPA's Standards
https://www.nap.edu/[...]
The National Academies Press
[23]
서적
TOXICOLOGICAL PROFILE FOR FLUORIDES, HYDROGEN FLUORIDE, AND FLUORINE
https://www.atsdr.cd[...]
U.S. DEPARTMENT OF HEALTH AND HUMAN SERVICES Public Health Service Agency for Toxic Substances and Disease Registry
[24]
논문
A new perspective on metals and other contaminants in fluoridation chemicals
2014
[25]
간행물
Aluminum Compounds Review of Toxicological Literature Abridged Final Report
https://ntp.niehs.ni[...]
National Institute of Environmental Health Sciences
2001-10
[26]
서적
Inorganic Chemistry
Academic Press
2001
[27]
서적
RubberBible92nd
[28]
서적
Greenwood&Earnshaw2nd
[29]
서적
CRC Handbook of Chemistry and Physics
https://books.google[...]
CRC Press
2003-06-19
[30]
서적
RubberBible92nd
[31]
논문
Zur kenntnis von AlF3 und InF3 [1]
[32]
서적
RubberBible92nd
[33]
서적
HazMat Data: For First Response, Transportation, Storage, and Security
https://books.google[...]
John Wiley & Sons
2005-03-04
[34]
웹인용
Aluminum Fluoride
https://pubchem.ncbi[...]
National Institute of Health
2017-10-12
[35]
간행물
PGCH
[36]
웹인용
ALUMINIUM FLUORIDE (ANHYDROUS) International Chemical Safety Cards (ICSC)
https://www.cdc.gov/[...]
2015-07-22
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com
